根据题目描述,我们需要对由氢气(H₂)、二氧化碳(CO₂)和一氧化碳(CO)中一种或几种组成的混合气体进行成分确定。实验现象与结论分析如下:
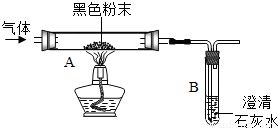
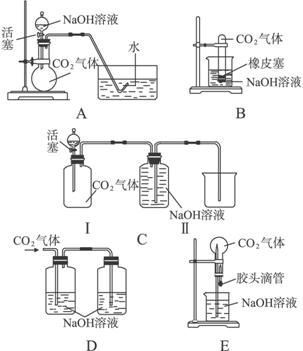
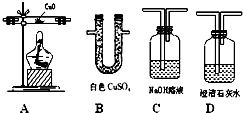
实验①将气体通过澄清石灰水(氢氧化钙溶液),未出现浑浊现象。澄清石灰水遇二氧化碳会生成碳酸钙白色沉淀,从而变浑浊。未出现浑浊,说明混合气体中不含二氧化碳(CO₂),或者二氧化碳含量极少不足以产生明显沉淀(但题目通常默认可检出,故认为不含CO₂)。
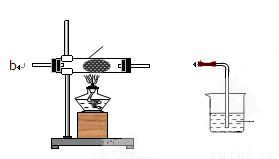
实验②将气体通过灼热的氧化铜(CuO),观察到有红色固体生成。氧化铜为黑色,在加热条件下可被还原性气体还原为红色的铜单质。氢气(H₂)和一氧化碳(CO)均具有还原性,反应方程式分别为:
H₂ + CuO → Cu + H₂O
CO + CuO → Cu + CO₂
因此,该现象说明混合气体中至少含有氢气(H₂)和一氧化碳(CO)中的一种或两种。
实验③将气体点燃后通入澄清石灰水,但题目未给出具体现象。基于实验①和②,我们已排除CO₂,并确定存在H₂和/或CO。若气体点燃后通入石灰水出现浑浊,则说明燃烧产物中有CO₂,可推断原混合气体中含有一氧化碳(CO),因为CO燃烧生成CO₂。若未出现浑浊,则可能只含氢气(H₂),因为氢气燃烧只生成水。但题目中实验③未描述现象,因此需要结合常见推断逻辑:由于实验②已证明气体具有还原性,且实验①排除了CO₂,通常可假设气体可能为H₂、CO或两者混合物。为完全确定成分,实验③是关键——若点燃后通入石灰水变浑浊,则证明含CO;若不变浑浊,则只含H₂。但基于题目信息不完整,最合理的结论是:混合气体中一定不含CO₂,一定含有H₂和CO中的至少一种。
若实验③点燃后通入石灰水出现浑浊,则气体成分为CO或H₂与CO的混合物;若实验③无浑浊,则气体成分为H₂。但题目未提供实验③现象,因此无法唯一确定,需补充信息。
另外,用户输入末尾提及“液体分离及纯净设备销售”,这与气体成分分析无直接关联,可能是误输入或无关信息。在化学实验中,气体净化与分离设备可用于制备或提纯气体,但本实验未涉及该过程。
因此,根据给定实验①和②,气体成分可能为:①只有H₂;②只有CO;③H₂和CO的混合物。需要实验③的现象来最终判定。